מבנה האטומים - חלקיקים יסודיים של חומר, אלקטרונים, פרוטונים, נויטרונים
 כל הגופים הפיזיים בטבע עשויים מסוג של חומר הנקרא חומר. חומרים מחולקים לשתי קבוצות עיקריות - חומרים פשוטים ומורכבים.
כל הגופים הפיזיים בטבע עשויים מסוג של חומר הנקרא חומר. חומרים מחולקים לשתי קבוצות עיקריות - חומרים פשוטים ומורכבים.
חומרים מורכבים הם אותם חומרים שבאמצעות תגובות כימיות ניתן לפרק לחומרים אחרים ופשוטים יותר. בניגוד לחומרים מורכבים, חומרים פשוטים הם כאלה שלא ניתן לפרק כימית לחומרים פשוטים עוד יותר.
דוגמה לחומר מורכב הוא מים, שבאמצעות תגובה כימית ניתן לפרק לשני חומרים אחרים ופשוטים יותר - מימן וחמצן. לגבי שני האחרונים, כבר לא ניתן לפרק אותם כימית לחומרים פשוטים יותר ולכן הם חומרים פשוטים, או במילים אחרות, יסודות כימיים.
במחצית הראשונה של המאה ה-19, הייתה הנחה במדע כי יסודות כימיים הם חומרים ללא שינוי שאין להם קשר משותף זה עם זה. עם זאת, המדען הרוסי D.I. Mendeleev (1834 - 1907) לראשונה בשנת 1869חושף את מערכת היחסים של יסודות כימיים, ומראה כי המאפיין האיכותי של כל אחד מהם תלוי במאפיין הכמותי שלו - משקל אטומי.
בחקר התכונות של יסודות כימיים, D.I. מנדלייב הבחין שתכונותיהם חוזרות על עצמן מעת לעת בהתאם למשקל האטומי שלהם. הוא הראה מחזוריות זו בצורה של טבלה, שנכנסה למדע תחת השם "טבלת היסודות המחזורית של מנדלייב".
להלן הטבלה המחזורית המודרנית של יסודות כימיים של מנדלייב.
אטומים
על פי תפיסות מדעיות מודרניות, כל יסוד כימי מורכב מאוסף של חלקיקי החומר (החומר) הקטנים ביותר הנקראים אטומים.
אטום הוא החלק הקטן ביותר של יסוד כימי שלא ניתן עוד לפירוק כימי לחלקיקי חומר אחרים, קטנים ופשוטים יותר.
אטומים של יסודות כימיים בעלי אופי שונה נבדלים זה מזה בתכונותיהם הפיזיקליות-כימיות, במבנה, בגודל, במסה, במשקל אטומי, באנרגיה שלהם ובכמה תכונות אחרות. למשל, אטום המימן שונה מאוד בתכונותיו ובמבנהו מאטום החמצן, והאחרון מאטום האורניום וכן הלאה.
אטומים של יסודות כימיים מתגלים כקטנים ביותר בגודלם. אם נניח באופן מותנה שלאטומים יש צורה כדורית, אז הקטרים שלהם חייבים להיות שווה למאה מיליוניות הסנטימטר. לדוגמה, קוטרו של אטום מימן - האטום הקטן ביותר בטבע - הוא מאה מיליונית הסנטימטר (10-8 ס"מ), וקוטר האטומים הגדולים, למשל, אטום האורניום, אינו עולה על שלוש מאות. מיליוניות הסנטימטר (3 10-8 ס"מ).לכן, אטום המימן קטן פי כמה מכדור הרדיוס של סנטימטר אחד, כפי שהאחרון קטן מהכדור.
בשל גודלם הקטן מאוד של אטומים, גם המסה שלהם קטנה מאוד. לדוגמה, המסה של אטום מימן היא m = 1.67· 10-24 פירוש הדבר שגרם אחד של מימן מכיל כ-6·1023 אטומים.
עבור יחידת המדידה הקונבנציונלית של המשקלים האטומיים של יסודות כימיים, נלקח 1/16 ממשקל אטום חמצן. בהתאם למשקל האטומי הזה של יסוד כימי, נקרא מספר מופשט, המציין כמה פעמים משקלו של יסוד כימי נתון הוא יותר מ-1/16 ממשקל אטום חמצן.
בטבלה המחזורית של היסודות של D.I. Mendeleev, הנתונים האטומיים של כל היסודות הכימיים (ראה את המספר מתחת לשם היסוד). מטבלה זו אנו רואים שהאטום הקל ביותר הוא אטום המימן, שיש לו משקל אטומי של 1.008. המשקל האטומי של פחמן הוא 12, חמצן הוא 16 וכן הלאה.
באשר ליסודות הכימיים הכבדים יותר, משקלם האטומי עולה על המשקל האטומי של המימן ביותר ממאתיים. אז הערך האטומי של כספית הוא 200.6, רדיום הוא 226 וכן הלאה. ככל שסדר המספרים התפוס על ידי יסוד כימי בטבלה המחזורית של היסודות גבוה יותר, המשקל האטומי גדול יותר.
רוב המשקלים האטומיים של יסודות כימיים מבוטאים כמספרים שברים. זה מוסבר במידה מסוימת על ידי העובדה שאלמנטים כימיים כאלה מורכבים מקבוצה של כמה סוגי אטומים בעלי משקל אטומי שונה אך עם אותן תכונות כימיות.
יסודות כימיים שתופסים את אותו מספר בטבלה המחזורית של היסודות ולכן בעלי אותן תכונות כימיות אך בעלי משקל אטומי שונה נקראים איזוטופים.
איזוטופים נמצאים ברוב היסודות הכימיים, ישנם שני איזוטופים, סידן – ארבעה, אבץ – חמישה, בדיל – אחד עשר ועוד. איזוטופים רבים מתקבלים באמצעות אמנות, לחלקם יש חשיבות מעשית רבה.
חלקיקי חומר יסודיים
במשך זמן רב האמינו שהאטומים של יסודות כימיים הם הגבול של חלוקת החומר, כלומר, כביכול, "אבני הבניין" היסודיות של היקום. המדע המודרני דוחה השערה זו בכך שהוא קובע שהאטום של כל יסוד כימי הוא מצרף של חלקיקי חומר קטנים אפילו יותר מהאטום עצמו.
על פי תורת האלקטרונים של מבנה החומר, האטום של כל יסוד כימי הוא מערכת המורכבת מגרעין מרכזי שסביבו מסתובבים חלקיקים "אלמנטריים" של החומר הנקראים אלקטרונים. גרעיני האטומים, על פי השקפות מקובלות, מורכבים מקבוצה של חלקיקי חומר "אלמנטריים" - פרוטונים ונייטרונים.
על מנת להבין את מבנה האטומים ואת התהליכים הפיזיקליים-כימיים בהם, יש צורך לפחות להכיר בקצרה את המאפיינים הבסיסיים של החלקיקים היסודיים המרכיבים את האטומים.
נקבע שאלקטרון הוא חלקיק אמיתי עם המטען החשמלי השלילי הקטן ביותר שנצפה בטבע.
אם נניח באופן מותנה שלאלקטרון כחלקיק יש צורה כדורית, אז קוטר האלקטרון צריך להיות שווה ל-4 ·10-13 ס"מ, כלומר, הוא קטן בעשרות אלפי מונים מקוטר כל אטום.
לאלקטרון, כמו לכל חלקיק חומר אחר, יש מסה. "מסת המנוחה" של האלקטרון, כלומר המסה שיש לו במצב של מנוחה יחסית, שווה ל-mo = 9.1 · 10-28 G.
"מסת המנוחה" הקטנה ביותר של האלקטרון מעידה על כך שתכונות האינרציה של האלקטרון חלשות ביותר, מה שאומר שהאלקטרון, בהשפעת כוח חשמלי מתחלף, יכול להתנודד בחלל בתדירות של מיליארדים רבים של תקופות. שְׁנִיָה.
מסת האלקטרון כל כך קטנה שצריך 1027 יחידות כדי לייצר גרם אחד של אלקטרונים. על מנת לקבל לפחות מושג פיזיקלי על המספר הגדול הזה, ניתן דוגמה. אם ניתן היה לסדר גרם אחד של אלקטרונים בקו ישר קרוב זה לזה, אז הם היו יוצרים שרשרת באורך ארבעה מיליארד קילומטרים.
מסת האלקטרון, כמו כל מיקרו-חלקיק חומר אחר, תלויה במהירות התנועה שלו. לאלקטרון במצב מנוחה יחסי יש "מסת מנוחה" בעלת אופי מכני, הדומה למסה של כל גוף פיזי. לגבי "מסת התנועה" של האלקטרון, שעולה ככל שמהירות תנועתו עולה, היא ממקור אלקטרומגנטי. זה נובע מהימצאותו של שדה אלקטרומגנטי באלקטרון נע כסוג של חומר בעל מסה ואנרגיה אלקטרומגנטית.
ככל שהאלקטרון נע מהר יותר, ככל שהתכונות האינרציאליות של השדה האלקטרומגנטי שלו באות לידי ביטוי, כך גדלה המסה של האחרון ובהתאם גם האנרגיה האלקטרומגנטית שלו. מאחר שהאלקטרון עם השדה האלקטרומגנטי שלו מייצג מערכת חומר אחת מחוברת אורגנית, הוא היא טבעית שמסת התנע של השדה האלקטרומגנטי של האלקטרון המיוחסת ישירות לאלקטרון עצמו.
לאלקרון, בנוסף לתכונות של חלקיק, יש גם תכונות גל.בניסוי נקבע שזרימת אלקטרונים, כמו זרימת אור, מתפשטת בצורה של תנועה דמוית גל. אופי תנועת הגל של זרימת האלקטרונים בחלל מאושרת על ידי תופעות של הפרעות ודיפרקציה של גלי אלקטרונים.
הפרעה אלקטרונית היא תופעת סופרפוזיציה של רצונות אלקטרונים זה על זה ודיפרקציה של אלקטרונים - זוהי התופעה של גלי אלקטרונים המתכופפים בקצוות של חריץ צר שדרכו עוברת אלומת האלקטרונים. לכן, האלקטרון אינו רק חלקיק, אלא "גל חלקיקים", שאורכו תלוי במסה ובמהירות של האלקטרון.
נקבע כי האלקטרון, בנוסף לתנועת התרגום שלו, מבצע גם תנועה סיבובית סביב צירו. סוג זה של תנועת אלקטרונים נקרא "ספין" (מהמילה האנגלית "ספין" - ציר). כתוצאה מתנועה זו, האלקטרון, בנוסף לתכונות החשמליות הנובעות מהמטען החשמלי, מקבל גם תכונות מגנטיות, המזכירות מבחינה זו מגנט אלמנטרי.
פרוטון הוא חלקיק אמיתי עם מטען חשמלי חיובי השווה בערכו המוחלט למטען החשמלי של אלקטרון.
מסת הפרוטון היא 1.67 ·10-24 r, כלומר גדולה פי 1840 בערך מ"מסת המנוחה" של האלקטרון.
שלא כמו אלקטרון ופרוטון, לנייטרון אין מטען חשמלי, כלומר הוא חלקיק "אלמנטרי" נייטרלי חשמלית של חומר. מסת הנייטרון כמעט שווה למסה של הפרוטון.
האלקטרונים, הפרוטונים והנייטרונים המרכיבים את האטומים מקיימים אינטראקציה זה עם זה. בפרט, אלקטרונים ופרוטונים מושכים זה את זה כחלקיקים בעלי מטענים חשמליים מנוגדים.במקביל, אלקטרונים מאלקטרון ופרוטונים מפרוטונים דוחים כחלקיקים בעלי אותם מטענים חשמליים.
כל החלקיקים הטעונים חשמלית הללו מקיימים אינטראקציה דרך השדות החשמליים שלהם. שדות אלו הם סוג מיוחד של חומר המורכב מאוסף של חלקיקי חומר יסודי הנקראים פוטונים. לכל פוטון יש כמות מוגדרת בהחלט של אנרגיה (קוונטית אנרגיה) הטבועה בו.
האינטראקציה של חלקיקים מחומרי חומר טעונים חשמלית מתרחשת באמצעות חילופי פוטונים זה עם זה. כוח האינטראקציה של חלקיקים טעונים חשמלית נקרא בדרך כלל הכוח החשמלי.
גם ניוטרונים ופרוטונים בגרעיני האטומים מקיימים אינטראקציה זה עם זה. עם זאת, האינטראקציה הזו ביניהם כבר לא מתרחשת דרך שדה חשמלי, שכן הנייטרון הוא חלקיק נייטרלי חשמלי של חומר, אלא דרך מה שנקרא שדה גרעיני.
שדה זה הוא גם סוג מיוחד של חומר המורכב מאוסף של חלקיקי חומר יסודי הנקראים מזוונים... האינטראקציה של נויטרונים ופרוטונים מתרחשת באמצעות חילופי מזוונים זה עם זה. כוח האינטראקציה בין נויטרונים לפרוטונים נקרא כוח גרעיני.
הוכח כי כוחות גרעיניים פועלים בגרעיני האטומים במרחקים קטנים במיוחד - כ-10-13 ס"מ.
כוחות גרעיניים עולים בהרבה על הכוחות החשמליים של דחייה הדדית של פרוטונים בגרעין של אטום. זה מוביל לעובדה שהם מסוגלים לא רק להתגבר על כוחות הדחייה ההדדית של פרוטונים בתוך גרעיני האטומים, אלא גם ליצור מערכות חזקות מאוד של גרעינים מאוסף הפרוטונים והנייטרונים.
היציבות של הגרעין של כל אטום תלויה ביחס של שני כוחות מתנגשים - גרעיני (משיכה הדדית של פרוטונים וניוטרונים) וחשמלי (דחייה הדדית של פרוטונים).
כוחות גרעיניים רבי עוצמה הפועלים בגרעיני האטומים תורמים להפיכת נויטרונים ופרוטונים זה לתוך זה. אינטראקציות אלו של נויטרונים ופרוטונים מתרחשות כתוצאה משחרור או ספיגה של חלקיקים אלמנטריים קלים יותר, למשל מזוונים.
החלקיקים הנחשבים על ידינו נקראים אלמנטריים מכיוון שהם אינם מורכבים ממצרף של חלקיקי חומר אחרים ופשוטים יותר. אך יחד עם זאת, אסור לשכוח שהם מסוגלים להפוך זה לזה, להתעורר על חשבון האחר. לפיכך, חלקיקים אלה הם כמה תצורות מורכבות, כלומר, הטבע היסודי שלהם מותנה.
מבנה כימי של אטומים
האטום הפשוט ביותר במבנה שלו הוא אטום המימן. הוא מורכב מאוסף של שני חלקיקים יסודיים בלבד - פרוטון ואלקטרון. הפרוטון במערכת אטומי המימן ממלא תפקיד של גרעין מרכזי שסביבו מסתובב אלקטרון במסלול מסוים. באיור. 1 מציג באופן סכמטי מודל של אטום המימן.
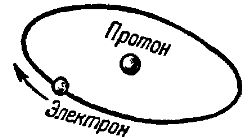
אורז. 1. תרשים מבנה אטום המימן
מודל זה הוא רק קירוב גס של המציאות. העובדה היא שלאלקטרון כ"גל חלקיקים" אין נפח תחום בחדות מהסביבה החיצונית. וזה אומר שצריך לדבר לא על איזה מסלול ליניארי מדויק של האלקטרון, אלא על סוג של ענן אלקטרונים. במקרה זה, האלקטרון תופס לרוב קו אמצעי כלשהו של הענן, שהוא אחד ממסלוליו האפשריים באטום.
יש לומר שהמסלול של האלקטרון עצמו אינו משתנה לחלוטין ונייח באטום - הוא גם, עקב השינוי במסה של האלקטרון, מבצע תנועה סיבובית מסוימת. לכן, התנועה של אלקטרון באטום היא מסובכת יחסית. מכיוון שלגרעין אטום המימן (פרוטון) והאלקטרון הסובב סביבו יש מטענים חשמליים הפוכים, הם מושכים זה את זה.
במקביל, האנרגיה החופשית של האלקטרון, המסתובבת סביב גרעין האטום, מפתחת כוח צנטריפוגלי שנוטה לסלק אותו מהגרעין. לכן, הכוח החשמלי של משיכה הדדית בין גרעין האטום והאלקטרון והכוח הצנטריפוגלי הפועל על האלקטרון הם כוחות מנוגדים.
בשיווי משקל, האלקטרון שלהם תופס מיקום יציב יחסית במסלול כלשהו באטום. מכיוון שמסת האלקטרון קטנה מאוד, אזי כדי לאזן את כוח המשיכה לגרעין האטום, עליו להסתובב במהירות עצומה השווה לכ-6·1015 סיבובים בשנייה. המשמעות היא שאלקטרון במערכת של אטום מימן, כמו כל אטום אחר, נע לאורך מסלולו במהירות לינארית העולה על אלף קילומטרים לשנייה.
בתנאים רגילים, אלקטרון מסתובב באטום מהסוג במסלול הקרוב ביותר לגרעין. יחד עם זאת, יש לו את הכמות המינימלית האפשרית של אנרגיה. אם מסיבה כזו או אחרת, למשל, בהשפעת חלקיקי חומר אחרים שפלשו למערכת האטומית, האלקטרון יעבור למסלול מרוחק יותר מהאטום, אז כבר תהיה לו כמות מעט יותר גדולה של אנרגיה.
עם זאת, האלקטרון נשאר במסלול החדש הזה לפרק זמן לא משמעותי, ולאחר מכן הוא מסתובב בחזרה למסלול הקרוב ביותר לגרעין האטום.במהלך הקורס הזה הוא מוותר על האנרגיה העודפת שלו בצורה של קוואנטום של קרינה מגנטית - אנרגיית קרינה (איור 2).
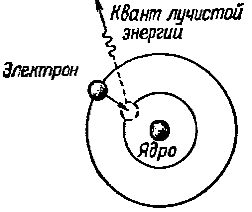
אורז. 2. כאשר אלקטרון עובר ממסלול מרוחק למסלול קרוב יותר לגרעין האטום, הוא פולט קוואנטום של אנרגיית קרינה
ככל שהאלקטרון מקבל יותר אנרגיה מבחוץ, כך הוא נע למסלול הרחוק ביותר מגרעין האטום, וכמות האנרגיה האלקטרומגנטית שהוא פולט גדול יותר כשהוא מסתובב למסלול הקרוב ביותר לגרעין.
על ידי מדידת כמות האנרגיה שפולט האלקטרון במהלך המעבר ממסלולים שונים למסלול הקרוב ביותר לגרעין האטום, ניתן היה לקבוע שאלקטרון במערכת של אטום מימן, כמו במערכת של כל אחד אחר. אטום, לא יכול ללכת למסלול אקראי, לכיוון שנקבע בקפדנות בהתאם לאנרגיה הזו שהוא מקבל בהשפעת כוח חיצוני. המסלולים שאלקטרון יכול לתפוס באטום נקראים אורביטלים מותרים.
מכיוון שהמטען החיובי של גרעין אטום המימן (מטען הפרוטון) והמטען השלילי של האלקטרון שווים מבחינה מספרית, המטען הכולל שלהם הוא אפס. המשמעות היא שאטום המימן במצבו הרגיל הוא חלקיק נייטרלי מבחינה חשמלית.
זה נכון לגבי האטומים של כל היסודות הכימיים: האטום של כל יסוד כימי במצבו הרגיל הוא חלקיק נייטרלי מבחינה חשמלית בשל השוויון המספרי של מטענים חיוביים ושליליים.
מכיוון שגרעין אטום מימן מכיל רק חלקיק "יסודי" אחד - פרוטון, מה שנקרא מספר המסה של גרעין זה שווה לאחד. מספר המסה של הגרעין של אטום של יסוד כימי כלשהו הוא המספר הכולל של פרוטונים וניוטרונים המרכיבים את הגרעין הזה.
מימן טבעי מורכב בעיקר מאוסף של אטומים שמספר המסה שלהם שווה לאחד. עם זאת, הוא מכיל גם סוג אחר של אטומי מימן, עם מספר מסה שווה לשניים. הגרעינים של אטומי המימן הכבדים הללו, הנקראים דיוטרונים, מורכבים משני חלקיקים, פרוטון ונייטרון. איזוטופ זה של מימן נקרא דאוטריום.
מימן טבעי מכיל כמויות קטנות מאוד של דאוטריום. על כל ששת אלפים אטומי מימן קלים (מספר המסה שווה לאחד), יש רק אטום דאוטריום אחד (מימן כבד). יש איזוטופ נוסף של מימן, מימן סופר-כבד הנקרא טריטיום. בגרעין של אטום של איזוטופ מימן זה, ישנם שלושה חלקיקים: פרוטון ושני נויטרונים, הקשורים יחדיו על ידי כוחות גרעיניים. מספר המסה של גרעין אטום טריטיום הוא שלוש, כלומר, אטום הטריטיום כבד פי שלושה מאטום המימן הקל.
למרות שלאטומים של איזוטופי מימן יש מסות שונות, עדיין יש להם את אותן תכונות כימיות, למשל, מימן קל, הנכנס לתגובה כימית עם חמצן, יוצר איתו חומר מורכב - מים. כמו כן, האיזוטופ של המימן, דאוטריום, מתחבר עם חמצן ויוצר מים, שבניגוד למים רגילים, נקראים מים כבדים. מים כבדים נמצאים בשימוש נרחב בייצור אנרגיה גרעינית (אטומית).
לכן, התכונות הכימיות של אטומים אינן תלויות במסה של הגרעינים שלהם, אלא רק במבנה של מעטפת האלקטרונים של האטום. מכיוון שלאטומים של מימן קל, דאוטריום וטריטיום יש מספר זהה של אלקטרונים (אחד לכל אטום), לאיזוטופים הללו יש אותן תכונות כימיות.
לא סתם היסוד הכימי מימן תופס את המספר הראשון בטבלה המחזורית של היסודות.העובדה היא שיש קשר כלשהו בין המספר של כל יסוד בטבלה המחזורית של היסודות לבין גודל המטען על גרעין האטום של אותו יסוד. ניתן לנסח זאת כך: המספר הסידורי של כל יסוד כימי בטבלה המחזורית של היסודות שווה מספרית למטען החיובי של הגרעין של אותו יסוד, ולכן למספר האלקטרונים המסתובבים סביבו.
מכיוון שמימן תופס את המספר הראשון בטבלה המחזורית של היסודות, פירוש הדבר שהמטען החיובי של גרעין האטום שלו שווה לאחד ושאלקטרון אחד מסתובב סביב הגרעין.
היסוד הכימי הליום נמצא במקום השני בטבלה המחזורית של היסודות. זה אומר שיש לו מטען חשמלי חיובי של הגרעין השווה לשתי יחידות, כלומר, הגרעין שלו חייב להכיל שני פרוטונים, ובקליפת האלקטרונים של האטום - שתי אלקטרודות.
הליום טבעי מורכב משני איזוטופים - הליום כבד וקל. מספר המסה של הליום כבד הוא ארבע. המשמעות היא שבנוסף לשני הפרוטונים שהוזכרו לעיל, חייבים להיכנס לגרעין של אטום ההליום הכבד שני נויטרונים נוספים. באשר להליום הקל, מספר המסה שלו הוא שלוש, כלומר, בנוסף לשני פרוטונים, עוד נויטרון אחד צריך להיכנס להרכב הגרעין שלו.
נמצא כי בהליום טבעי מספר אטומי ההליום הקל הוא כמיליון מאטומי הגן הכבד. באיור. 3 מציג מודל סכמטי של אטום הליום.
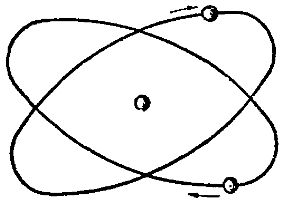
אורז. 3. תרשים מבנה אטום ההליום
הסיבוך הנוסף של מבנה האטומים של יסודות כימיים נובע מעלייה במספר הפרוטונים והנייטרונים בגרעיני האטומים הללו ובמקביל מעלייה במספר האלקטרונים המסתובבים סביב הגרעינים (איור 4). באמצעות הטבלה המחזורית של היסודות, קל לקבוע את מספר האלקטרונים, הפרוטונים והנייטרונים המרכיבים אטומים שונים.
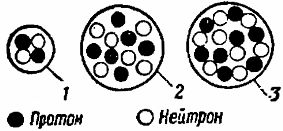
אורז. 4. סכימות של בניית גרעיני אטום: 1 - הליום, 2 - פחמן, 3 - חמצן
המספר הקבוע של יסוד כימי שווה למספר הפרוטונים בגרעין האטום ובמקביל למספר האלקטרונים המסתובבים סביב הגרעין. באשר למשקל האטומי, הוא שווה בקירוב למספר המסה של האטום, כלומר למספר הפרוטונים והנייטרונים שנלקחו יחד בגרעין. לכן, על ידי הפחתת ממשקל האטום של יסוד מספר השווה למספר האטומי של היסוד, ניתן לקבוע כמה נויטרונים נמצאים בגרעין נתון.
נקבע כי גרעינים של יסודות כימיים קלים, בעלי מספר שווה של פרוטונים וניוטרונים בהרכבם, נבדלים בחוזק גבוה מאוד, שכן הכוחות הגרעיניים בהם גדולים יחסית. לדוגמה, הגרעין של אטום הליום כבד הוא עמיד ביותר מכיוון שהוא מורכב משני פרוטונים ושני נויטרונים הקשורים יחדיו על ידי כוחות גרעיניים רבי עוצמה.
גרעיני האטומים של יסודות כימיים כבדים יותר מכילים כבר בהרכבם מספר לא שווה של פרוטונים וניוטרונים, וזו הסיבה שהקשר שלהם בגרעין חלש יותר מאשר בגרעין של יסודות כימיים קלים. ניתן לפצל את הגרעינים של יסודות אלו בקלות יחסית כאשר מופצצים ב"קליעים" אטומיים (נייטרונים, גרעיני הליום וכו').
באשר ליסודות הכימיים הכבדים ביותר, במיוחד הרדיואקטיביים, הגרעינים שלהם מאופיינים בחוזק כה נמוך עד שהם מתפוררים באופן ספונטני לחלקיהם המרכיבים. לדוגמה, אטומים של היסוד הרדיואקטיבי רדיום, המורכב משילוב של 88 פרוטונים ו-138 נויטרונים, מתפרקים באופן ספונטני, והופכים לאטומים של היסוד הרדיואקטיבי ראדון. האטומים של האחרונים, בתורם, מתפרקים לחלקים המרכיבים שלהם, עוברים לאטומים של יסודות אחרים.
לאחר שהכרנו בקצרה את החלקים המרכיבים את גרעיני האטומים של יסודות כימיים, הבה נבחן את המבנה של קליפות האלקטרונים של האטומים. כפי שאתה יודע, אלקטרונים יכולים להסתובב סביב גרעיני האטומים רק במסלולים מוגדרים בהחלט. יתר על כן, הם כל כך מקובצים במעטפת האלקטרונים של כל אטום שניתן להבחין בין קליפות אלקטרונים בודדות.
כל קליפה יכולה להכיל מספר מסוים של אלקטרונים, שאינם עולים על מספר מסוים בהחלט. כך, למשל, במעטפת האלקטרונים הראשונה הקרובה לגרעין של אטום יכולים להיות מקסימום שני אלקטרונים, בשנייה - לא יותר משמונה אלקטרונים וכו'.
לאוטומים האלה שבהם קליפות האלקטרונים החיצוניות מלאות לחלוטין יש את מעטפת האלקטרונים היציבה ביותר. המשמעות היא שאטום מחזיק בחוזקה את כל האלקטרונים שלו ואינו צריך לקבל כמות נוספת מהם מבחוץ. לדוגמה, לאטום הליום יש שני אלקטרונים הממלאים לחלוטין את מעטפת האלקטרון הראשונה, ובאטום ניאון יש עשרה אלקטרונים, מתוכם שני הראשונים ממלאים לחלוטין את מעטפת האלקטרון הראשונה והשאר - השני (איור 5).
אורז. 5. תרשים מבנה אטום הניאון
לכן, לאטומי הליום וניאון יש קליפות אלקטרוניות יציבות למדי, הם לא נוטים לשנות אותם בשום דרך כמותית. יסודות כאלה הם אינרטיים מבחינה כימית, כלומר, הם אינם נכנסים לאינטראקציה כימית עם יסודות אחרים.
עם זאת, לרוב היסודות הכימיים יש אטומים שבהם קליפות האלקטרונים החיצוניות אינן מלאות לחלוטין באלקטרונים. לדוגמה, לאטום אשלגן יש תשעה עשר אלקטרונים, שמונה עשר מהם ממלאים לחלוטין את שלוש הקליפות הראשונות, והאלקטרון התשעה עשר נמצא בקליפת האלקטרון הבאה, הלא מלאה. המילוי החלש של מעטפת האלקטרון הרביעי באלקטרונים מוביל לכך שגרעין האטום מחזיק בצורה חלשה מאוד את החיצוני ביותר - האלקטרון התשעה עשר, ולכן ניתן להסיר את האחרון בקלות מהאטום. …
או, למשל, לאטום החמצן יש שמונה אלקטרונים, שניים מהם ממלאים לחלוטין את הקליפה הראשונה, ושישה הנותרים ממוקמים בקליפה השנייה. לפיכך, להשלמת בניית מעטפת האלקטרון השנייה באטום החמצן, חסרים לה שני אלקטרונים בלבד. לכן, אטום החמצן לא רק מחזיק בחוזקה את ששת האלקטרונים שלו בקליפה השנייה, אלא יש לו גם את היכולת למשוך אליו שני אלקטרונים חסרים כדי למלא את מעטפת האלקטרונים השנייה שלו. את זה הוא משיג על ידי שילוב כימי עם האטומים של יסודות כאלה שבהם האלקטרונים החיצוניים קשורים בצורה חלשה לגרעיניהם.
יסודות כימיים שלאטומים שלהם אין שכבות אלקטרונים חיצוניות מלאות לגמרי באלקטרונים, הם, ככלל, פעילים מבחינה כימית, כלומר, הם נכנסים ברצון לאינטראקציה כימית.
אז, האלקטרונים באטומים של היסודות הכימיים מסודרים בסדר מוגדר בהחלט, וכל שינוי בסידור המרחבי שלהם או בכמות שלהם במעטפת האלקטרונים של האטום מוביל לשינוי בתכונות הפיזיקליות-כימיות של האחרון.
השוויון של מספר האלקטרונים והפרוטונים במערכת האטומית הוא הסיבה לכך שהמטען החשמלי הכולל שלה הוא אפס. אם השוויון של מספר האלקטרונים והפרוטונים במערכת האטומית מופר, אז האטום הופך למערכת טעונה חשמלית.
אטום במערכת אשר מאזן המטענים החשמליים המנוגדים שלו מופר בשל העובדה שאיבד חלק מהאלקטרונים שלו או להיפך, רכש עודף מהם, נקרא יון.
להיפך, אם אטום רוכש מספר עודף של אלקטרונים, הוא הופך ליון שלילי. למשל, אטום כלור שקיבל אלקטרון אחד נוסף הופך ליון כלור שלילי בעל מטען יחיד Cl-... אטום חמצן שקיבל שני אלקטרונים נוספים הופך ליון חמצן שלילי טעון כפול O, וכן הלאה.
אטום שהפך ליון הופך למערכת טעונה חשמלית ביחס לסביבה החיצונית. וזה אומר שהאטום התחיל להחזיק בשדה חשמלי, יחד איתו הוא יוצר מערכת חומר יחידה, ודרך השדה הזה הוא מבצע אינטראקציה חשמלית עם חלקיקי חומר טעונים חשמלית אחרים - יונים, אלקטרונים, גרעינים בעלי מטען חיובי של אטומים, וכו '
היכולת של יונים שונים למשוך זה את זה היא הסיבה שהם משתלבים בצורה כימית, ויוצרים חלקיקים מורכבים יותר של חומר - מולקולות.
לסיכום, יש לציין כי מימדי האטום גדולים מאוד בהשוואה לממדים של החלקיקים האמיתיים מהם הם מורכבים. הגרעין של האטום המורכב ביותר, יחד עם כל האלקטרונים, תופס מיליארדית מנפח האטום. חישוב פשוט מראה שאם ניתן ללחוץ מטר מעוקב פלטינה כל כך חזק עד שהחללים התוך-אטומיים והבין-אטומיים ייעלמו, אז יתקבל נפח השווה למילימטר מעוקב אחד בערך.
